Определение
Загрязнение твердыми частицами — это присутствие в инфузионном растворе посторонних подвижных и нерастворимых частиц. Эти частицы могут быть различных размеров, определяемыми при визуальном осмотре (размер частиц > 50 мкм) или невидимые (размер частиц 2–50 мкм). Для обнаружения в растворе частиц размером менее 50 мкм требуется применение специального оборудования.
Знаете ли вы, что...

2 Anonymus [No authors listed]. (2004) Risks due to particles in infusion therapy--experts promote use of infusion filters. Krankenpfl J. 2004; 42(3-4): 97
3 Lehr HA, Brunner J, Rangoonwala R, Kirkpatrick CJ. (2002) Particulate matter contamination of intravenous antibiotics aggravates loss of functional capillary density in postischemic striated muscle. Am J Respir Crit Care Med; 165:514-520
Причины
Известно несколько причин загрязнения инфузионных растворов. Чаще всего источником загрязнения твердыми частицами являются лекарства, находящиеся в таких упаковках, как флаконы, стеклянные ампулы, предварительно заполненные флаконы или смешанные растворы, варианты использования которых разнообразны. В результате значительное количество разных видов частиц попадает в инфузионный раствор.
Стекло
Стеклянные ампулы являются источниками повышенной опасности с точки зрения загрязнения твердыми частицами, так как во время вскрытия ампулы осколки стекла могут попасть в раствор 3. При использовании игл размером 18G для забора лекарственного средства из ампул, осколки стекла оказываются в шприце или в инфузионном флаконе, что приводит к попаданию частиц стекла в вену пациента.
Риск загрязнения частицами стекла сохраняется и при обычном введении лекарства через инъекционный порт внутривенного катетера 3, 4.
Пластик
Контаминация пластиком чаще всего происходит:
- от попадания частичек пластика самого инфузионного контейнера;
- во время использования инъекционного порта острыми устройствами.
Резина
Источником загрязнения растворов твердыми частицами резины чаще всего являются инфузионные флаконы. Прокол резиновой пробки флакона иглой с целью забора лекарства приводит к попаданию кусочков резины в раствор и, в дальнейшем, аспирации лекарства, загрязненного частицами резины. Затем, во время инфузии или инъекции, загрязненный раствор попадает в сосудистое русло пациента 5.
Труднорастворимые лекарства
Зачастую, причиной образования труднорастворимых лекарственных частиц становится несовместимость некоторых лекарственных средств. Речь идет о нежелательной реакции между лекарственным средством и растворителем в момент введения лекарства в инфузионный флакон. Нежелательная реакция может возникнуть также при взаимодействии нескольких лекарственных средств, введенных в инфузионную линию или венозный катетер непосредственно во время инфузии. В результате реакции между лекарственными средствами происходит выпадение осадка и образование труднорастворимых частиц 6, 7.
Последствия
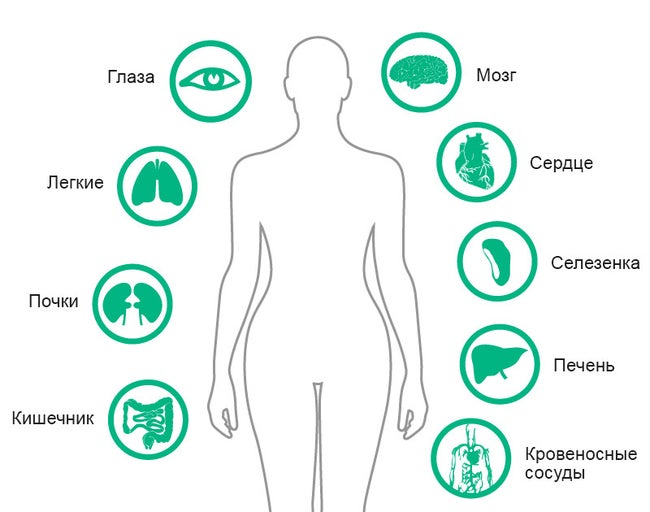
В случае, если не используется инфузионный фильтр, все типы частиц, находящиеся внутри инфузионной линии, попадают непосредственно в организм человека (рис. 1). Частицы пластика, стекла или резины могут вызвать серьезные патологические процессы, особенно, если пациент уже находится на лечении.
Повреждение различных органов (легкие, почки, печень, селезенка) подтверждены исследованиями 1, 6, особенно последствия выражены у тяжелобольных пациентов 8–11. Пациенты с уже имеющимся патологическим процессом особенно чувствительны к повреждающему действию твердых частиц, т. к. они могут вызвать нарушение микроциркуляции в пораженных органах и системах 8, 11.
Попадание стеклянных частиц от ампул во время инъекции или инфузии в вену вызывает флебит. При флебите наблюдается местное повышение температуры, болезненность, припухлость и покраснение в месте инфузии. Повреждение различных органов: легких, почек, печени и селезенки подтверждены исследованиями.
Финансовые затраты
Загрязнение твердыми частицами пластика, стекла, резины во время инфузии или инъекции становится причиной серьезных осложнений для пациента, что приводит к возрастанию стоимости лечения и увеличению сроков пребывания в стационаре.
Расчет затрат
При анализе дополнительных затрат на лечение осложнений, связанных с воздушной эмболией, учитываются фактически понесенные расходы на лечение и пребывание в стационаре. Затраты рассчитывались исходя из среднесуточной стоимости лечения в стационаре.
Данные, приведенные в таблице (рис. 2), демонстрируют результаты подсчета расходов для лечения осложнений, связанных с попаданием твердых частиц в кровоток пациента.
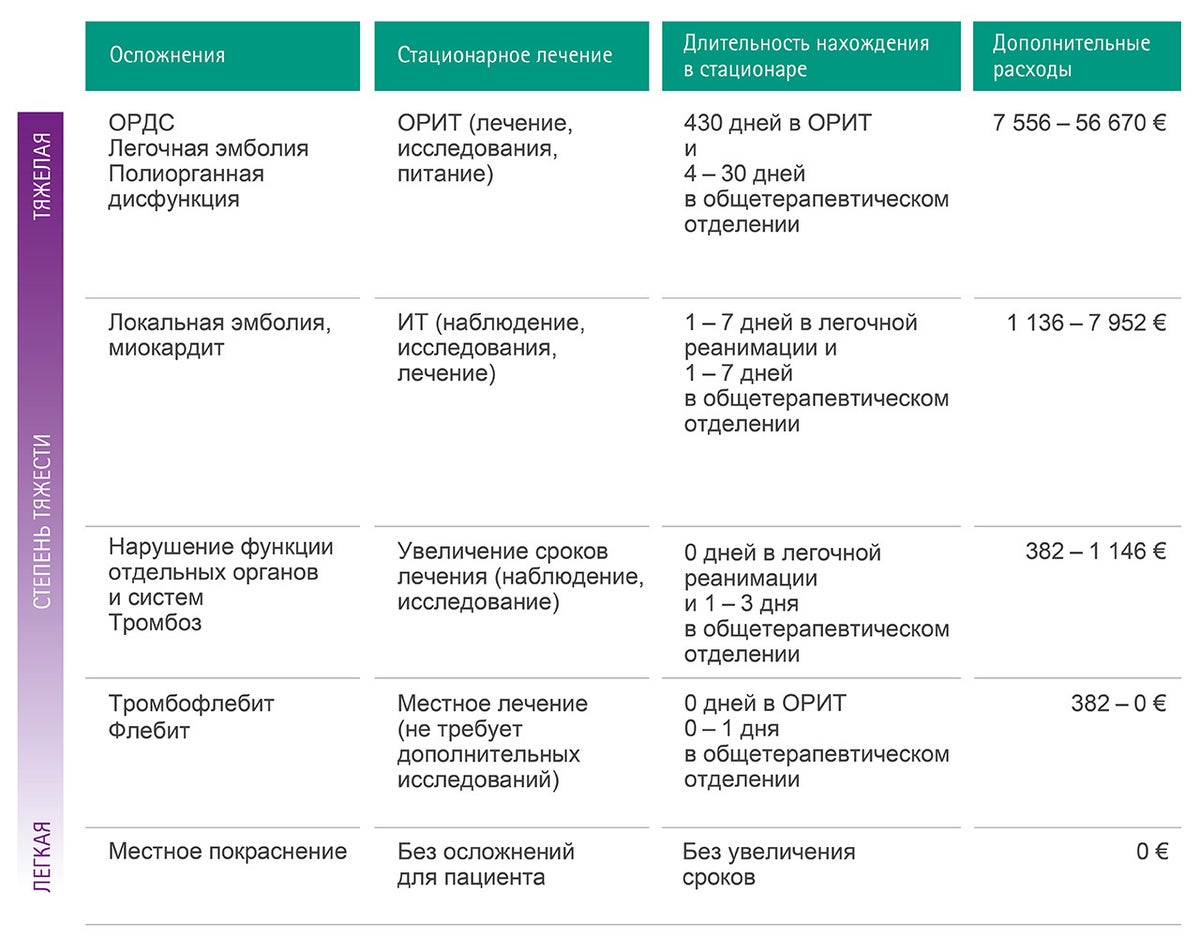
Профилактика загрязнения инфузионных и инъекционных растворов твердыми частицами позволит сэкономить значительные финансовые средства стационара. В случае предупреждения осложнения тяжелой степени, которое требует лечения в отделении реанимации, больница может сэкономить до 56 670 € в каждом конкретном случае16–19.
Профилактические мероприятия
Профилактические мероприятия, предупреждающие попадание твердых частичек в организм пациента:
- использование инфузионных флаконов и систем, изготовленных из высококачественных материалов, безопасных, с точки зрения возможного образования твердых частиц;
- использование вместо стеклянных ампул пластиковых контейнеров;
- использование специальных инфузионных систем и фильтров;
- при смешивании лекарств необходимо учитывать возможную лекарственную несовместимость.
Риск контаминации твердыми частицами может быть снижен путем использования инфузионных фильтров и фильтров для забора лекарственных средств из стеклянных ампул. Такие фильтры могут устранить появление:
- загрязнения твердыми частицами;
- микробной контаминации;
- воздушной эмболии.
В случае если частицы уже попали в инфузионный раствор, использование инфузионных фильтров позволит не допустить попадания этих частиц в линию, которая ведет к доступу пациента. Кроме того, если во время инфузии пропускная способность фильтра снижается по причине загрязнения частицами, инфузия автоматически останавливается.
Типы фильтров, используемых для инфузии
- Для стандартных инфузионных растворов с размером пор мембраны фильтра 0,2 мкм14
- Для жировых эмульсий или готовой смеси для парентерального питания с размером пор мембраны фильтра 1,2 мкм14
- ISO 8536-4 (для инфузионных систем) рекомендует применять фильтрацию раствора для защиты пациента. Инфузионные системы должны иметь встроенный фильтр с размером пор мембраны фильтра 15 мкм
Организация The British Pharmaceutical Nutrition Group (BPNG) разработала рекомендации по предупреждению попадания во время инфузии посторонних частиц в организм пациента 14, 15.
- Забор лекарств из стеклянных ампул для добавления в парентеральное питание должен производиться через устройства для аспирации, оснащенные фильтром с размером пор не более 5 мкм. Инъекционные фильтры и аспирационные канюли снижают риск попадания посторонних частиц в вену пациента (рис. 3).
- Соответствующие фильтры должны использоваться у пациентов, которым длительное время осуществляется парентеральное питание, пациентов со сниженным иммунитетом, новорожденных, детей и пациентов, которым осуществляется парентеральное питание в домашних условиях.
- Фильтры с размером пор 1,2 мкм должны использоваться для переливания растворов жировых эмульсий, готовых парентеральных смесей, содержащих липиды. Замена данных фильтров должна производиться каждые 24 часа.
- Инфузионные фильтры должны подсоединяться к инфузионной системе как можно ближе к венозному доступу пациента.
Устройства для обеспечения безопасности
Список литературы
1 Werner BP, Winter G. (2015) Particle contamination of parenteralia and in-line filtration of proteinaceous drugs. Int J Pharm;496(2):250-67
2 Doessegger L, Mahler HC, Szczesny P, Rockstroh H, Kallmeyer G, Langenkamp A, Herrmann J, Famulare J. (2012) The potential clinical relevance of visible particles in parenteral drugs. J Pharm Sci; 101(8): 2635-44
3 Lee KR, Chae YJ, Cho SE, Chung SJ. (2011) A strategy for reducing particulate contamination on opening glass ampoules and development of evaluation methods for its application. Drug Dev Ind Pharm; 37(12): 1394-401
4 Lye ST, Hwang NC. (2003) Glass particle contamination: is it here to stay? Anaesthesia; 58(1): 93-4
5 Roth JV. (2007) How to enter a medication vial without coring. Anesth Analg; 104(6): 1615
6 Boehne M, Jack T, Köditz H, Seidemann K, Schmidt F, Abura M, Bertram H, Sasse M. (2013) In-line filtration minimizes organ dysfunction: new aspects from a prospective, randomized, controlled trial. BMC Pediatr; 13 : 21
7 Ortolani GA, Russell RL, Angelbeck JA, Schaffer J, Wenz B. (2004) Contamination control in nursing with filtration. Part 1: filters applied to intravenous fluids and point-of-use hospital water. J Infus Nurs; 27(2): 89-103
8 Anonymus [No authors listed]. (2004) Risks due to particles in infusion therapy--experts promote use of infusion filters. Krankenpfl J. 2004; 42(3-4): 97
9 Jack T, Boehne M, Brent BE, Hoy L, Köditz H, Wessel A, Sasse M. (2012) In-line filtration reduces severe complications and length of stay on pediatric intensive care unit: a prospective, randomized, controlled trial. Intensive Care Med; 38(6): 1008-1
10 Oie S, Kamiya A. (2005) Particulate and microbial contamination in in-use admixed parenteral nutrition solutions. Biol Pharm Bull; 28(12): 2268-70
11 Lehr HA, Brunner J, Rangoonwala R, Kirkpatrick CJ. (2002) Particulate matter contamination of intravenous antibiotics aggravates loss of functional capillary density in postischemic striated muscle. Am J Respir Crit Care Med; 165:514-520
http://www.ncbi.nlm.nih.gov/pubmed/11850345
12 Yorioka K, Oie S, Oomaki M, Imamura A, Kamiya A. (2006) Particulate and microbial contamination in in-use admixed intravenous infusions. Biol Pharm Bull;29(11):2321-3
http://www.ncbi.nlm.nih.gov/pubmed/17077539
13 Nassaji-Zavareh M, Ghorbani R. Peripheral intravenous catheter-related phlebitis and related risk factors. Singapore Med J. 2007 Aug;48(8):733-6
14 Ball PA. (2003) Intravenous in-line filters: filtering the evidence. Curr Opin Clin Nutr Metab Care; 6(3): 319-25
15 Bethune K Allwood M, Grainger C, Wormleighton C; British Pharmaceutical Nutrition Group Working Party. (2001) Use of filters during the preparation and administration of parenteral nutrition: position paper and guidelines prepared by a British pharmaceutical nutrition group working party. Nutrition;17(5):403-8
16 Gianino MM, Vallino A, Minniti D, Abbona F, Mineccia C, Silvaplana P and Zotti CM. A method to determine hospital costs associated with nosocomial infections (transl). Ann Ig 2007; 19(4): 381-92
http://www.ncbi.nlm.nih.gov/pubmed/17937330
17 Kossovsky N, Cole P, Zackson DA. Giant cell myocarditis associated with silicone. An unusual case of biomaterials pathology discovered at autopsy using X-ray energy spectroscopic techniques. Am J Clin Pathol 1990; 93(1): 148-52
http://www.ncbi.nlm.nih.gov/pubmed/2294695
18 Walpot H, Franke RP, Burchard WG, Agtermkamp C, Müller FG, Mittermayer C, Kalff G. The filter effectiveness of common 15-micron filters (DIN 58362). II: Scanning electron microscopy and roentgen analysis. Infusionstherapie 1989; 16(3): 133-9
http://www.ncbi.nlm.nih.gov/pubmed/2503453
19 Preston ST, Hegadoren K. Glass contamination in parenterally administered medication. J Adv Nurs 2004; 48(3): 266-70